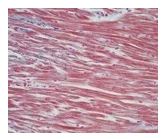
در مطالعهای که اخیراً در Nature منتشر شده است، محققان ارتباط فیبروبلاست ایمنی را در بیماریهای قلبی انسان و مدلهای موش بررسی کردند.
آنها دریافتند که سیگنال دهی اینترلوکین 1 بتا (IL-1β) بین ماکروفاژها و فیبروبلاست های گیرنده کموکاین C-C نوع 2 (CCR2+) به فیبروز قلبی کمک می کند و اختلال در سیگنال دهی IL-1β به طور بالقوه باعث کاهش فیبروز و بهبود عملکرد قلب می شود.
پس زمینه
التهاب و فیبروز، عوامل کلیدی در اختلال عملکرد قلب، در بیماری های مختلف قلبی، به ویژه انفارکتوس میوکارد (MI) و کاردیومیوپاتی شایع هستند. علیرغم اهمیت بالینی آن، کمبود استراتژی های درمانی برای هدف قرار دادن فیبروز وجود دارد. در حالی که مدلهای موش برای شناسایی زیرشاخههای فیبروبلاستهای دخیل در آسیب قلبی استفاده شدهاند، جمعیت فیبروبلاستهای دقیق که باعث ایجاد فیبروز در قلب انسان میشوند، همراه با مکانیسمهای تنظیمی آنها، نامشخص است.
مدل های پیش بالینی به طور کامل زیرگروه های فیبروبلاست انسانی را نمی گیرند. فنآوریهای توالییابی با توان بالا، مانند توالییابی اسید ریبونوکلئیک تک هستهای (snRNA-seq)، درک ما را از بیماریهای قلبی ارتقا دادهاند، اما این مطالعات فاقد دادههای دقیق ترانسکریپتومی، اپی ژنتیکی و پروتئومی سلولی هستند.
علاوه بر این، چالشها در دستیابی به بافت قلب انسان تازه، از مطالعات مقیاس بزرگ با استفاده از توالییابی تک سلولی یا مبتنی بر اپی توپ برای کشف کامل تعاملات ایمنی-فیبروبلاست در فیبروز قلبی جلوگیری کرده است.
در مطالعه حاضر، محققان از نمایهسازی سلولی رونوشتها و اپی توپها (CITE-seq)، توالییابی چندومیک و رونویسی فضایی برای تجزیه و تحلیل جمعیتهای فیبروبلاست و تعاملات ایمنی در قلب انسان و موش استفاده کردند.
در مورد مطالعه
فیبروز قلبی با استفاده از توالی یابی تک سلولی پیشرفته بر روی نمونه های بطن چپ از اهداکنندگان سالم و بیماران نارسایی قلبی با MI حاد (4 نفر)، کاردیومیوپاتی ایسکمیک (ICM، n = 6) و کاردیومیوپاتی غیر ایسکمیک (NICM, n) مورد بررسی قرار گرفت. = 6).
در مجموع 143804 سلول به دست آمد و حالت های فیبروبلاست متمایز از طریق خوشه بندی نزدیکترین همسایه وزنی، بیان ژن دیفرانسیل (DGE)، و فراخوانی اوج (MACS2) شناسایی شد. محققان آنتولوژی ژن و تجزیه و تحلیل KEGG را در کنار رونویسی فضایی برای ارزیابی توزیع فیبروبلاست، مقایسه فیبروبلاست های بیمار و سالم با بیان دیفرانسیل شبه توده انجام دادند.
مدلسازی پویا به مشخص کردن مسیرهای تمایز فیبروبلاست کمک کرد که از طریق ردیابی نسب ژنتیکی در موش تأیید شد. علاوه بر این، دسترسی کروماتین برای درک چشم انداز اپی ژنتیکی فیبروبلاست های مرتبط با بیماری مورد تجزیه و تحلیل قرار گرفت.
استفاده از غربالگری تک سلولی B برای افزایش کشف آنتیبادی، کتاب الکترونیکی Sphere Fluidics بهترین شیوهها و نکاتی را در مورد چگونگی افزایش کشف آنتیبادی با استفاده از غربالگری تک سلولی به اشتراک میگذارد.
آخرین نسخه را دانلود کنید
مدلهای تجربی مختلف مورد ارزیابی قرار گرفتند و تکنیکهای انتقال برچسب برای نقشهبرداری فیبروبلاستهای موش بر روی مجموعه دادههای انسانی، از جمله فیبروبلاستهای کشتشده انسانی که با فاکتور رشد تغییر شکل بتا (TGFβ) یا IL-1β تیمار شدهاند، استفاده شد. بیان IL-1β در سلول های میلوئیدی در مدل های آسیب ارزیابی شد و موش های اصلاح شده ژنتیکی برای کشف نقش بالقوه IL-1β در ایجاد فیبروز تولید شدند.
نتایج و بحث
در مجموع 11 نوع سلول متمایز، به ویژه سلول های میلوئیدی و T گسترش یافته، در بافت قلب انسان به دنبال MI حاد، با تغییرات قابل توجه در هفته اول شناسایی شد. تجزیه و تحلیل شبه حجیم DGE تفاوت قابل توجهی را بین اهداکنندگان سالم و شرایط نارسایی قلبی در انواع مختلف سلول نشان داد. توالی یابی چندومی پروفایل های دسترسی کروماتین منحصر به فردی را در کاردیومیوسیت ها، سلول های میلوئیدی و فیبروبلاست ها ارائه کرد و فاکتورهای رونویسی مرتبط با عناصر تنظیمی را شناسایی کرد که ممکن است به شبکه های تنظیم کننده ژن خاص بیماری قلبی کمک کنند.
سیزده حالت سلول فیبروبلاست متمایز شناسایی شد، به ویژه F2 (میوفیبروبلاست) و F9 (پروتئین فعال کننده فیبروبلاست و فیبروبلاست های ترشح کننده پریوستین [FAP/POSTN)، که در نارسایی قلبی پس از MI غنی شدند. فیبروبلاستهای F9، مرتبط با بازسازی ماتریکس خارج سلولی و برهمکنشهای ایمنی، به عنوان یک حالت بیماریزای بالقوه نقش دارند. رونویسی فضایی نشان داد که ایالات مختلف فیبروبلاست در انفارکتوس، مرز، و مناطق دور میوکارد، با فیبروبلاستهای F9 با سلولهای میلوئیدی کلوکالیزه میشوند.
مشخص شد که فیبروبلاست ها عمدتاً به سمت حالات F2، F4 و F9 با افزایش بیان FAP در دودمان F9 تغییر می کنند. تجزیه و تحلیل عامل رونویسی MEOX1 را به عنوان یک تنظیم کننده کلیدی دودمان F9 شناسایی کرد. تجزیه و تحلیل دسترسی کروماتین تغییرات قابل توجهی را در فیبروبلاست های نارسایی قلبی نشان داد که ژن هایی مانند POSTN و RUNX1 را به شبکه تنظیمی فیبروبلاست های F9 در فیبروز قلبی مرتبط می کند.
نگاشت داده های سکته قلبی موش به CITE-seq انسانی شباهت های زیادی را در بین جمعیت های فیبروبلاست نشان داد. درمان با مهارکننده BRD4 JQ1 نشان داد که از دست دادن فیبروبلاستهای F9 عملکرد قلب و فیبرو را بهبود میبخشد.
منبع:news-medical